一针见「耗子尾汁」:手把手教会你「小鼠尾静脉注射」操作技巧!
小鼠尾静脉注射,是动物实验中非常重要的一项实验技术,在小鼠静脉给药等实验中发挥着无可替代的作用。但是小鼠尾静脉十分纤细,不易观察,注射操作难度很高,「是个技术活儿」。
通过小鼠尾静脉的解剖结构来定位理想穿刺点
「知己知彼,百战不殆」。
成功的尾静脉注射离不开对小鼠尾部解剖结构的深入理解。有研究通过鼠尾横断面连续切片,报道了鼠尾的详细解剖结构[1],尽管研究使用的是大鼠而不是小鼠,但两者在尾部的解剖结构上十分相似,只是小鼠的尺寸更小。
从图1(左)中可以看到,鼠尾的血管主要由三条静脉(实心箭头)和一条中央动脉(空心箭头)组成,其余都是一些小的分支血管。中央动脉靠近腹侧,且位置较深,观察起来不容易,也不适用于穿刺。
背侧静脉和侧面的两条静脉位置较浅,都可以作为穿刺的候选。
其中,侧面的两条静脉相对背侧静脉更粗(尾部远端管腔内直径0.35 mm VS 0.18 mm),且走向更为清晰,通常作为穿刺的第一选择。简化的示意图1(右)可以帮助大家更好的理解小鼠尾部的解剖结构。
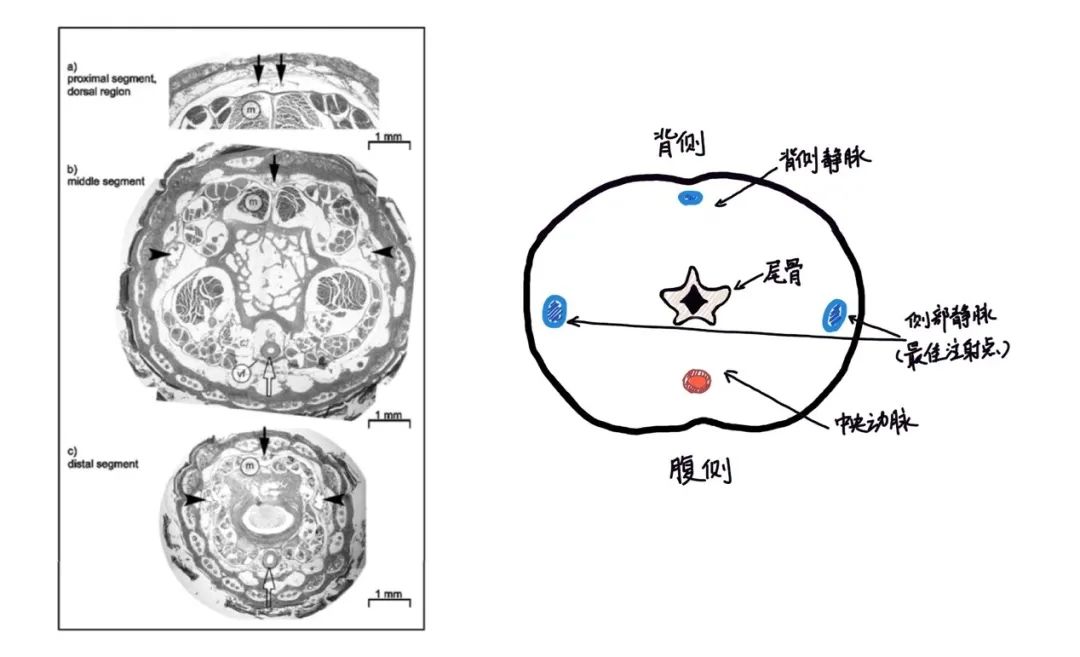
不止是静脉的选择,鼠尾穿刺位置的选择也同样重要。穿刺位置的血管首先要足够粗,在此基础上,位置越浅,越容易穿刺成功,这点后续还会讲到。
从图1(左)中可以看到,近端的血管位置较深,远端的血管位置较浅,但血管的管腔内径并没有随着鼠尾的变细而成比例的变细。在鼠尾远端,血管仍保持较粗的管腔内径。这就为定位一个理想的穿刺点提供了可能。
因此,我们一般首选离鼠尾远端约1/3的位置的侧面静脉进行穿刺。
选择合适的注射器
小鼠尾静脉的结构,导致我们对注射器提出了更高的要求。
我们需要选择针头足够细又有一定长度的注射器。那么,到哪里去找到合适的注射器呢?注射器针头粗细规格表示方法为数字+Gauge(G)。数字越大,代表针头越细。
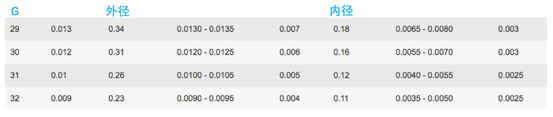
用于小鼠尾静脉的针头规格,最好在29G以上。目前,市面上容易买到的29G以上的注射器,主要是胰岛素注射器。其规格有29G,30G和32G。参数如表1。
但是32G的注射器针头长度太短,只有4 mm,并不方便操作,因此选择针头长度为8 mm和13 mm的30G和29G胰岛素注射器,是最为合适的。
注射前一个人可以用微型手电筒或LED小夜灯等紧贴尾静脉,在灯光的照射下,尾静脉会被很清晰的显示,此时,另一个人便进行注射操作。但该操作不易实现,需要多加练习,培养默契。
小鼠尾静脉注射的操作步骤:
1.首先要固定小鼠,最简单的固定方法就是把小鼠放在盒子里面,让它的尾巴伸在盒盖的外面,用手抓住小鼠尾巴,轻轻往外拽,就可以固定好小鼠了。这种固定方法,小鼠可以在盒子里面活动,固定的也不是很牢固,但是只要你尾静脉注射的手法很熟练,就足以用来注射了。还有的固定方法就是用一个小的圆筒,最好是金属做的,(可以在当地的铁匠铺,或者买白铁铺里面定做)首先是金属比较结实,而且可以用来固定在铁架台上,方便操作。圆筒的一段有个盖子可以拿下来,盖子中间有个小孔,可以让小鼠的尾巴伸出来(中间的小孔可以用胶布缠一下,防止锐利的边缘割伤小鼠尾巴)。另外一段可以用金属网的结构,网的形状可以做成子弹头的头端形状。网状结构可以让光线透近来,方便小鼠钻进圆筒里面。圆筒的长度约10cm,直径约 3~4cm,可以做个系列长度和直径的圆筒,适合不同大小的小鼠。
2.固定好小鼠后就是注射了,一般用一次性的1ml的注射器就可以了,玻璃 的1ml的注射器也可以用,针头用4号的就可以了。
3.注射前首先要让小鼠的血管充盈。可以采用75%的酒精棉球擦拭的方法或者采用温水浸泡的方法。若小鼠的血管很不清楚,推荐采用温水浸泡的方法,水温以不烫手为宜。温水浸泡2~3分钟后,取出小鼠尾巴,用干棉球擦拭。等一会儿,待血管充盈后,酒精棉球擦拭后就可以进针了。若血管还不充盈,可以反复用温水浸泡,切不可冒险注射,除非你手法很熟练,另当别论。
4.小鼠尾部共有四条血管,一般认为左右的两条静脉比较容易注射,多采用这两条静脉进针。一般要求进针部位靠近小鼠的尾端,这样若注射失败的话,还可以再向上选择进针点。但是进针部位也不可以太靠下,因为越往下,静脉越细,操作越难,一般以小鼠尾巴下三分之一的位置比较好。
5.最关键的就是进针了。进针时操作者左手食指和拇指固定住小鼠的尾巴,让小鼠的尾巴在经过拇指后向下弯曲,进针点靠近拇指指甲。针头和血管呈约30°角,针尖斜面朝上,轻轻挑刺入皮肤后针头立即和血管平行,一般情况下一次就可以进入血管,可以将针头刺入血管一大半,左右轻轻晃动针头,确定针头在血管内,就可以推注药液了,正常情况下,推注的过程应该没有明显阻力,血管也不会鼓起。推液时动作宜轻柔,若发现血管鼓起,那是针头没有刺入血管,需立即拔出针头。





